2024年1月28日,港股上市Biotech公司來凱醫藥發布公告,宣布旗下AKT抑制劑afuresertib聯合紫杉醇治療鉑耐藥卵巢癌的頂線數據公布。
該項名為PROFECTA-II的臨床研究(NCT04374630),是一項隨機、開放標簽、有效對照的二期臨床試驗,旨在評估afuresertib聯合紫杉醇治療與單獨紫杉醇對照對鉑耐藥卵巢癌(PROC)女性患者的療效和安全性。
該研究在美國和中國隨機入組了150名患者到試驗組和對照組,其主要終點為研究者評估的無進展生存期,次要終點包括總生存期、客觀緩解率和持續緩解時間。
試驗結果表明,afuresertib聯合紫杉醇周療可以降低疾病進展或死亡的風險(無進展生存期,PFS ),HR為0.744(95%CI: 0.502–1.102),但試驗沒有達到統計學意義。
在生物標志物陽性亞組( AKT磷酸化陽性,IHC>1 ) ( 占比37% )中,資料顯示,afuresertib聯合治療組顯著改善了PFS,中位PFS為5.4個月,而紫杉醇周療為2.9個月,HR為0.352(95%CI: 0.125–0.997)。
同時,次要終點總生存期(OS)在生物標志物亞組呈現積極的趨勢,其他次要終點也顯示,聯合治療組提高了客觀緩解率以及持續緩解時間。聯合治療組的安全性可控和可耐受,與藥物已知的安全特性基本保持一致。
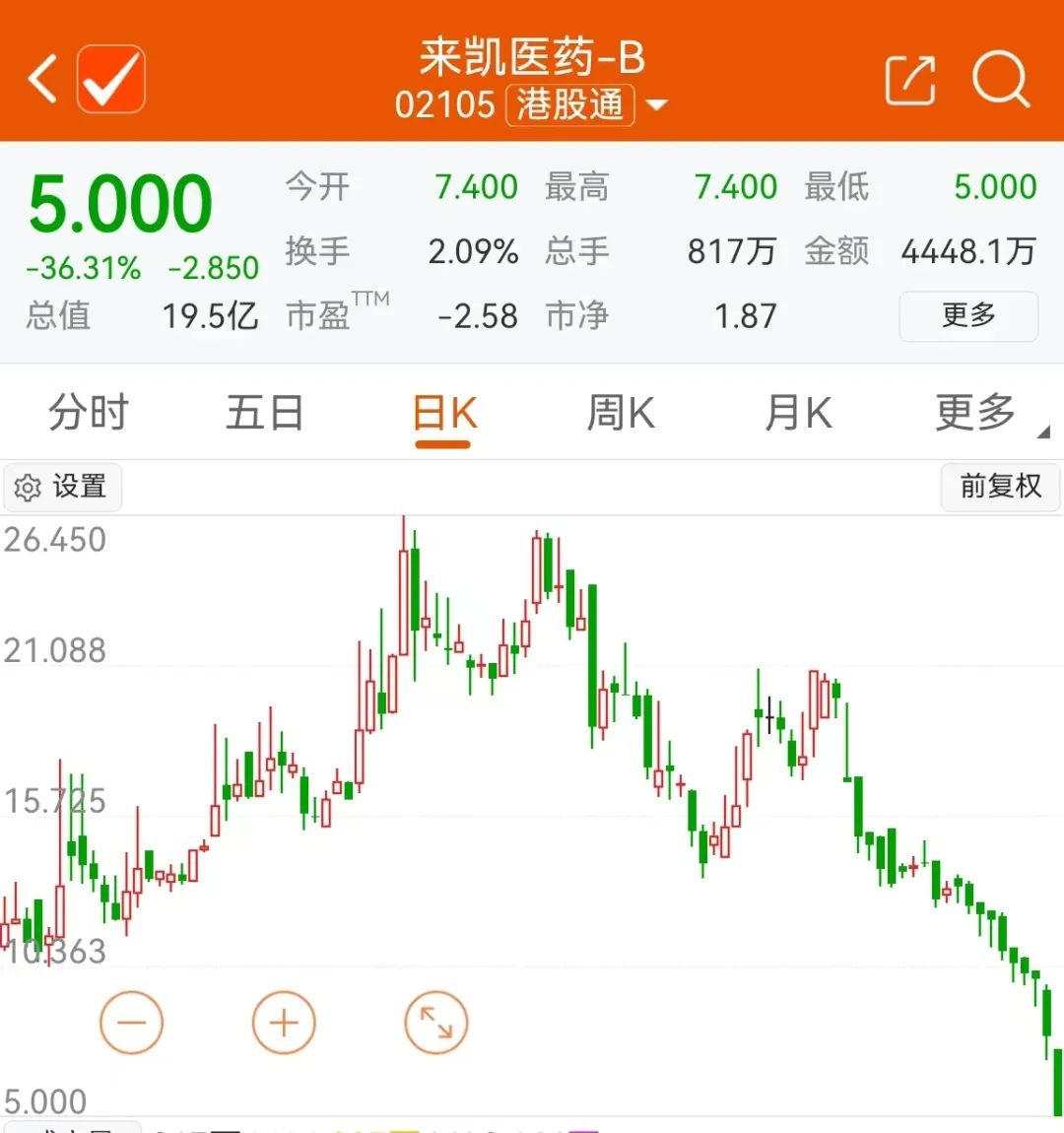
2024年1月29日當天,來凱醫藥股價暴跌36.31%,是當天港股18A板塊跌幅最大的個股。同時,自2023年11月以來,來凱醫藥的股價持續下跌,目前的股價,已經距離11月的25元/股的水平,跌去了大約80%。公開信息顯示,凱醫藥成立于2016年12月,是一家活躍于中國上海和美國新澤西的醫藥新銳公司,專注于腫瘤與肝病領域的突破性新藥研發。目前,該公司采取“雙線并舉”的新藥開發策略,一方面通過引進已經有臨床驗證(Proof of Concept)結果的新藥項目持續豐富自身產品管線,目前公司已經獲得諾華公司授予 4 項候選新藥的全球獨家授權;同時,公司自主開發的創新藥管線也同步推進。afuresertib(LAE002)是來凱醫藥從諾華公司引進全球獨家權益、此前已有一定的臨床驗證結果(Proof of Concept)的候選新藥,屬于新一代小分子泛AKT激酶強效抑制劑。afuresertib是一種口服、低納摩爾泛 AKT 激酶抑制劑,已被證明可抑制多種組織學的一系列腫瘤細胞系的增殖,包括乳腺、血液、結腸、卵巢和前列腺癌。afuresertib最早由GSK開發,先后完成了卵巢癌、胃癌、多發性骨髓瘤、黑色素瘤等適應癥領域的20多項臨床I/II 期研究。2014年,GSK與諾華達成了資產置換協議,afuresertib歸諾華所有。2018年,來凱從諾華授權引進 LAE002。目前,全球僅有阿斯利康的AKT抑制劑capivasertib成功獲批上市,此前來凱醫藥的afuresertib是臨床進度排名第二的AKT抑制劑。來凱醫藥表示,計劃與監管機構就該試驗結果討論,再決定下一步的注冊臨床路徑,詳細的試驗數據將在醫學會議上公布。
聲明:本文觀點僅代表作者本人,不代表煜森資本立場,歡迎在留言區交流補充。如需轉載,請注明文章作者和來源。如涉及作品內容、版權和其它問題,請在本平臺留言。